Цей легкий метал з сріблясто-білим відтінком в сучасному житті зустрічається майже повсюдно. Фізичні та хімічні властивості алюмінію дозволяють широко використовувати його в промисловості. Найвідоміші родовища – в Африці, Південній Америці, Карибському регіоні. У Росії місця видобутку бокситів є на Уралі. Світовими лідерами з виробництва алюмінію є Китай, РФ, Канада, США.
Видобуток Al
У природі цей сріблястий метал в силу своєї високої хімічної активності зустрічається лише у вигляді сполук. Найбільш відомі геологічні породи, що містять алюміній, – це боксити, глинозем, корунди, польові шпати. Промислове значення мають боксити і глинозем, саме родовища цих руд дозволяють добувати алюміній в чистому вигляді.
Властивості
Фізичні властивості алюмінію дозволяють легко витягувати заготовки цього металу в дріт і прокатувати в тонкі листи. Цей метал не є міцним, для підвищення даного показника при виплавці його легують різними добавками: міддю, кремнієм і магнієм, марганцем, цинком. Для промислового призначення важливо ще одне фізична властивість речовини алюмінію – це його здатність швидко окислюватися на повітрі. Поверхня виробу з алюмінію в природних умовах зазвичай покрита тонкою оксидною плівкою, яка ефективно захищає метал і перешкоджає його корозії. При знищенні цієї плівки сріблястий метал швидко окислюється, при цьому його температура помітно підвищується.
Внутрішня будова алюмінію
Фізичні та хімічні властивості алюмінію багато в чому залежать від його внутрішньої будови. Кристалічна решітка цього елемента є різновидом гранецентрованого куба.  Даний тип решітки притаманний багатьом металам, таким, як мідь, бром, срібло, золото, кобальт та інші. Висока теплопровідність і здатність проводити електрику зробили цей метал одним з найбільш затребуваних у світі. Інші фізичні властивості алюмінію, таблиця яких представлена нижче, розкривають повністю його властивості і показують сфери їх застосування.
Даний тип решітки притаманний багатьом металам, таким, як мідь, бром, срібло, золото, кобальт та інші. Висока теплопровідність і здатність проводити електрику зробили цей метал одним з найбільш затребуваних у світі. Інші фізичні властивості алюмінію, таблиця яких представлена нижче, розкривають повністю його властивості і показують сфери їх застосування.

Легування алюмінію
Фізичні властивості міді і алюмінію такі, що при додаванні до алюмінієвого сплаву деякої кількості міді його кристалічна решітка викривлюється, і міцність самого сплаву підвищується. На цій властивості Al засноване легування легких сплавів для підвищення їх міцності і стійкості до впливу агресивного середовища.
Пояснення процесу зміцнення лежить в поведінці атомів міді в кристалічній решітці алюмінію. Частинки Cu прагнуть випасти з кристалічної решітки Al, групуються на її особливих ділянках. 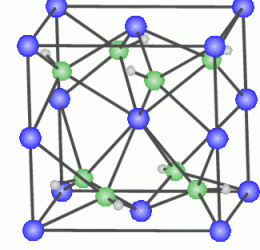 Там, де атоми міді утворюють скупчення, утворюється кристалічна решітка змішаного типу CuAl2 , в якій частинки сріблястого металу одночасно входять до складу і загальної кристалічної решітки алюмінію, і в склад решітки змішаного типу CuAl2. Сили внутрішніх зв’язків в спотвореній решітці набагато більше, ніж у звичайної. А отже, і міцність новоствореного речовини набагато вище.
Там, де атоми міді утворюють скупчення, утворюється кристалічна решітка змішаного типу CuAl2 , в якій частинки сріблястого металу одночасно входять до складу і загальної кристалічної решітки алюмінію, і в склад решітки змішаного типу CuAl2. Сили внутрішніх зв’язків в спотвореній решітці набагато більше, ніж у звичайної. А отже, і міцність новоствореного речовини набагато вище.
Хімічні властивості
Відомо взаємодія алюмінію з розведеними сірчаною і соляною кислотою. При нагріванні цей метал в них легко розчиняється. Холодна концентрована або сильно розбавлена азотна кислота розчиняє цей елемент. Водні розчини лугів активно впливають на речовину, в процесі реакції утворюючи алюмінати – солі, у складі яких є іони алюмінію. Наприклад:
Al2O3 +3H2O+2NaOH=2Na[Al(OH)4]
Вийшло в результаті реакції з’єднання носить назву тетрагидроксоалюминат натрію.
Тонка плівка на поверхні алюмінієвих виробів захищає цей метал не тільки від повітря, але і від води. Якщо цю тонку прибрати перешкоду, елемент стане бурхливо взаємодіяти з водою, виділяючи з неї водень.
2AL+6H2O= 2 AL (OH)3+3Н2?
Утворилася речовина називається гідроксидом алюмінію.
AL (OH)3 реагує з лугами, утворюючи кристали гідроксоалюмінат:
Al(OH)2+NaOH=2Na[Al(OH)4]
Якщо це хімічне рівняння скласти з попереднім, отримаємо формулу розчинення елемента в лужному розчині.
Al(OH)3+2NaOH+6H2O=2Na [Al(OH)4]+3H2?
Горіння алюмінію
Фізичні властивості алюмінію дозволяють йому вступати в реакцію з киснем. Якщо порошок цього металу або алюмінієву фольгу нагріти, то вона спалахує і горить білим сліпучим полум’ям. Наприкінці реакції утворюється оксид алюмінію Al2O3.
Глинозем
Отриманий оксид алюмінію має геологічне назва глинозем. У природних умовах він зустрічається у вигляді корунду – твердих прозорих кристалів. Корунд відрізняється високою твердістю, у шкалі твердих речовин його показник становить 9. Сам корунд безбарвний, але різні домішки можуть пофарбувати його в червоний і синій колір, так виходять дорогоцінні камені, які в ювелірній справі називаються рубінами і сапфірами.
Фізичні властивості оксиду алюмінію дозволяють вирощувати ці дорогоцінні камені в штучних умовах. Технічні дорогоцінне каміння використовуються не тільки для ювелірних прикрас, вони застосовуються в точному приладобудуванні, для виготовлення годинників та іншого. Широко використовуються штучні кристали рубіна і лазерних пристроїв.
Дрібнозерниста різновид корунду з великою кількістю домішок, нанесене на спеціальну поверхню, відома всім як наждак. Фізичні властивості оксиду алюмінію пояснюють високі абразивні властивості корунду, а також його твердість і стійкість до тертя.
Гідроксид алюмінію
Al2 (OH)3 є типовим амфотерним гідроксидом. У поєднанні з кислотою це речовина утворює сіль, що містить позитивно заряджені іони алюмінію, в лугах утворює алюмінати. Амфотерність речовини виявляється в тому, що він може поводитися і як кислота, і як луг. Це з’єднання може існувати і в желеподібному, і в твердому вигляді.  У воді практично не розчиняється, але вступає в реакцію з більшістю активних кислот і лугів. Фізичні властивості гідроксиду алюмінію використовуються в медицині, це популярне і безпечний засіб зниження кислотності в організмі, його застосовують при гастритах, дуоденітах, виразках. У промисловості Al2 (OH)3 використовується в якості адсорбенту, він чудово очищає воду і осаджує розчинені в ній шкідливі елементи.
У воді практично не розчиняється, але вступає в реакцію з більшістю активних кислот і лугів. Фізичні властивості гідроксиду алюмінію використовуються в медицині, це популярне і безпечний засіб зниження кислотності в організмі, його застосовують при гастритах, дуоденітах, виразках. У промисловості Al2 (OH)3 використовується в якості адсорбенту, він чудово очищає воду і осаджує розчинені в ній шкідливі елементи.
Промислове використання
Алюміній був відкритий у 1825 році. Спочатку цей метал цінувався вище золота і срібла. Це пояснювалося складністю його вилучення з руди. Фізичні властивості алюмінію та його здатність швидко утворювати захисну плівку на своїй поверхні утруднювали дослідження цього елемента. Лише в кінці 19 століття був відкритий зручний спосіб плавки чистого елемента, придатний для використання в промислових масштабах.

Легкість і здатність чинити опір корозії – унікальні фізичні властивості алюмінію. Сплави цього сріблястого металу застосовуються в ракетній техніці, в авто-, судно-, авіа – та приладобудуванні, у виробництві столових приладів і посуду.
Як чистий метал Al використовується при виготовленні деталей для хімічної апаратури, електропроводів і конденсаторів. Фізичні властивості алюмінію такі, що його електропровідність не так висока, як у міді, але цей недолік компенсується легкістю розглянутого металу, що дозволяє робити дроту з алюмінію більш товстими. Так, при однаковій електропровідності алюмінієвий дріт важить вдвічі меньше мідного.
Не менш важливим є застосування Al в процесі алітування. Так називається реакція насичення поверхні чавунного або сталевого вироби алюмінієм з метою захисту основного металу від корозії при нагріванні.
В даний час невідомі запаси алюмінієвих руд цілком порівнянні з потребами людей у цьому сріблястому металі. Фізичні властивості алюмінію можуть піднести ще чимало сюрпризів його дослідникам, а сфери застосування цього металу набагато ширше, ніж можна уявити.






