Можливо, ви ніколи не чули про ген PTEN, але він відіграє надзвичайно важливу роль у захисті нашого організму від раку. Цей невеликий, але могутній ген працює як своєрідний “гальмо” для клітинного росту. А що відбувається, коли це гальмо ламається? Давайте розберемося разом.
Що таке PTEN і чому він такий важливий?
PTEN (фосфатаза і тензин гомолог) – один з найчастіше мутованих пухлинносупресорних генів у онкології. Розташований на хромосомі 10q23, він кодує білок, який діє як молекулярний регулятор, контролюючи процеси клітинного росту, поділу та виживання.
За словами провідного генетика клініки Спіженка: “PTEN – це як головний диспетчер клітинного росту. Коли він працює правильно, клітини знають, коли зупинитися. Але мутації можуть порушити цю систему контролю.”
Білок PTEN функціонує через інгібування PI3K/AKT/mTOR сигнального шляху – одного з найважливіших шляхів контролю клітинного росту. Він видаляє фосфатні групи з PIP3 (фосфатидилінозитол-3,4,5-трифосфату), перетворюючи його на PIP2 і тим самим “вимикаючи” ростові сигнали.
Що робить PTEN унікальним, так це його подвійна функція: він працює і як ліпідна, і як білкова фосфатаза. Ліпідна активність більш відома, але білкова фосфатазна активність також критично важлива для пригнічення метастазування.
Спадкові синдроми, пов’язані з PTEN
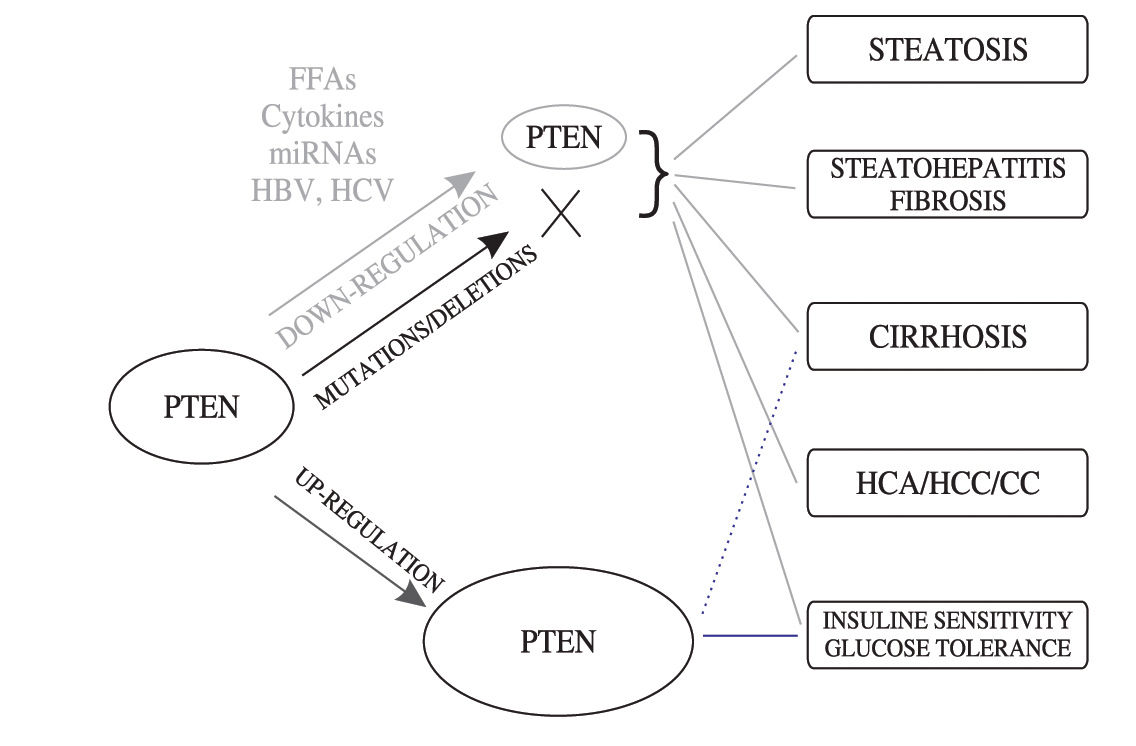
Герміналні мутації PTEN призводять до розвитку PTEN-асоційованих синдромів гамартомних пухлин (PHTS), які включають кілька різних станів.
- Синдром Коудена – найпоширеніший варіант PHTS. Пацієнти мають характерні ознаки: макроцефалію (збільшений розмір голови), численні гамартоми шкіри та слизових оболонок, а також підвищений ризик раку молочної залози (до 85%), ендометрія (до 30%) та щитоподібної залози.
- Синдром Баннаян-Райлі-Рувалькаба зазвичай проявляється в дитинстві макроцефалією, затримкою розвитку, пігментними плямами на статевому члені у хлопчиків та гамартомними поліпами кишківника.
Таблиця ризиків раку при PHTS:
| Тип раку | Пожиттєвий ризик | Середній вік початку |
| Молочна залоза | До 85% | 38-46 років |
| Ендометрій | 19-30% | 42-52 роки |
| Щитоподібна залоза | 35-38% | 37-42 роки |
| Нирки | 34% | 50+ років |
| Колоректальний | 9-16% | 50+ років |
Як зазначає онколог клініки Спіженка: “Пацієнти з мутаціями PTEN потребують особливої уваги. Ранній скринінг може врятувати життя, адже багато раків у них розвиваються в молодому віці.”
Соматичні мутації PTEN в пухлинах
Окрім спадкових синдромів, втрата функції PTEN часто трапляється в пухлинній тканині. Соматичні мутації або делеції PTEN виявляються в:
- 30-40% гліобластом;
- 20-30% раку ендометрія;
- 15-20% раку молочної залози;
- 10-15% раку передміхурової залози.
Цікаво, що PTEN демонструє дозозалежний ефект – навіть часткова втрата функції може призвести до онкогенезу. Це явище називається “haploinsufficiency”, коли недостатньо мати одну робочу копію гену.
Методи тестування PTEN
Сучасне тестування PTEN використовує різні технології залежно від клінічної ситуації:
- Секвенування нового покоління (NGS) – золотий стандарт для виявлення точкових мутацій та невеликих інделів. Цей метод аналізує всі кодуючі екзони PTEN та прилеглі інтронні послідовності.
- Мультиплексна лігазозалежна ампліфікація зонда (MLPA) використовується для виявлення великих делецій або дуплікацій, які можуть бути пропущені при стандартному секвенуванні.
- Іммуногістохімія дозволяє оцінити експресію білка PTEN в тканині пухлини. Втрата експресії може вказувати на функціональну інактивацію гену.
Особливості інтерпретації результатів
Результати тестування PTEN можуть бути складними для інтерпретації. Ось що варто знати:
- Патогенні мутації – чітко асоціюються з розвитком PHTS та підвищеним ризиком раку. Таким пацієнтам необхідне інтенсивне спостереження.
- Варіанти невизначеного значення (VUS) становлять особливий виклик. Не всі зміни в послідовності PTEN призводять до втрати функції. Функціональні дослідження допомагають класифікувати ці варіанти.
- Мозаїцизм – коли мутація присутня лише в частині клітин. Це може ускладнити діагностику, особливо якщо мутація виявляється в низькому відсотку клітин.
А чи знали ви, що PTEN може регулюватися не лише мутаціями?
Клінічні рекомендації для носіїв мутацій
Для осіб з патогенними мутаціями PTEN розроблені детальні протоколи спостереження:
Скринінг раку молочної залози:
- МРТ молочних залоз щорічно з 30-35 років
- Мамографія щорічно з 40 років
- Клінічне обстеження кожні 6 місяців
Скринінг раку ендометрія:
- УЗД органів малого таза щорічно з 30 років
- Біопсія ендометрія при показаннях
Скринінг раку щитоподібної залози:
- УЗД щитоподібної залози щорічно з 18 років
Терапевтичні можливості
Розуміння функції PTEN відкриває нові терапевтичні можливості:
- Інгібітори PI3K/AKT/mTOR можуть бути особливо ефективними при пухлинах з втратою PTEN. Препарати як еверолімус вже використовуються в клініці.
- Відновлення функції PTEN – експериментальний підхід, який включає генну терапію або реактивацію інактивованого PTEN.
- Синтетична летальність – стратегія, яка використовує специфічні вразливості PTEN-дефіцитних клітин.
Психологічні аспекти та генетичне консультування
Отримання позитивного результату тестування PTEN може спричинити значний психологічний стрес. Генетичне консультування допомагає:
- Зрозуміти персональні ризики
- Розробити план спостереження
- Обговорити репродуктивні питання
- Підготуватися до розмови з родиною
Важливо пам’ятати: носійство мутації PTEN не означає неминучий розвиток раку. Це означає підвищений ризик, який можна контролювати через регулярне спостереження та профілактичні заходи.
Тестування на мутації PTEN – важливий інструмент сучасної персоналізованої медицини. Воно дозволяє виявити осіб з високим ризиком раку та розробити індивідуальні стратегії профілактики. Хоча позитивний результат може викликати занепокоєння, ранне виявлення та регулярне спостереження значно покращують прогноз. Консультація з генетичним консультантом допоможе зрозуміти результати та розробити оптимальний план дій для збереження здоров’я.






